Asma Allergico Grave e Terapia biologica con anti-IgE (Omalizumab-Xolair).
Sono venti anni da quando è iniziata in Italia la terapia con anti-IgE (primo caso trattato a Napoli il 4 Dicembre 1998).
La patologia allergica ha un substrato genetico complesso e multifattoriale. L’atopia (allergia IgE-mediata) e l’asma hanno molti geni coinvolti in vari modi in ogni individuo. Non tutte le persone geneticamente a rischio svilupperanno allergia, ma perché la malattia si possa sviluppare la predisposizione genetica deve interagire con alcuni stimoli ambientali. Un’ipotesi generalmente accettata è che un anormale bilancio tra linfociti Th1 e Th2 ad uno stadio precoce della vita porti ad una risposta predominante di tipo Th2, caratteristica dell’allergia a substrato IgE-mediato. Una continua esposizione allergenica agisce poi come principale fattore di rischio per il successivo sviluppo di allergia, dal momento che le citochine prodotte dai Th2 favoriscono l’evoluzione delle cellule B verso la produzione di anticorpi IgE.
La ragione proposta per uno squilibrio a favore dei Th2 è una riduzione del principale stimolo, costituito da infezioni virali e batteriche, per la maturazione post-natale dei Th1. La riduzione di questi stimoli, determinata dai moderni standard di igiene pre e post-natale impedisce al sistema immune di innescare una corretta risposta Th1 e favorisce la risposta Th2 diretta verso la sintesi di IgE.
Una considerevole riduzione della mortalità infantile negli ultimi trenta anni è dovuta al declino delle infezioni, soprattutto quelle dell’apparato respiratorio e digestivo. Ciò, unito agli effetti della sterilizzazione del cibo e all’uso frequente di antibiotici a largo spettro per le comuni infezioni delle vie aeree superiori, ha ridotto però l’esposizione dei bambini a stimoli per la promozione dei linfociti Th1.
Inoltre tappeti e moquette, il riscaldamento centralizzato, ed i doppi infissi alle finestre sono diffusi, ma occorre tener presente che ciò favorisce la crescita di allergeni degli ambienti confinati come gli acari della polvere .Inoltre il fumo di tabacco va a stimolare la sintomatologia asmatica favorendo la riacutizzazione ed il peggioramento dei sintomi.
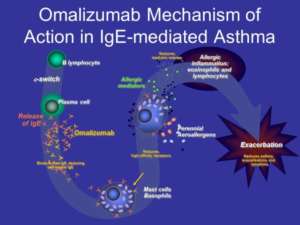
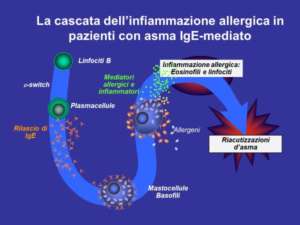
Anticorpi dell’Allergia, le IgE
Gli anticorpi o immunoglobuline (Ig) sono proteine sieriche coinvolte nella risposta immune specifica umana. La produzione di anticorpi da parte dei linfociti B maturi, definiti anche plasmacellule, è stimolata dalla presenza di sostanze non-self, definite antigeni. Il più abbondante tipo di immunoglobulina sierica è l’IgG. L’interazione tra Ig ed antigene induce una risposta infiammatoria di difesa. Le IgE sono una delle cinque classi di Ig nell’uomo. Le altre sono IgG,IgM,IgA e IgD Le risposte difensive stimolate dalle IgE inducono infiammazione che si esprimono clinicamente con tosse, broncocostrizione, secrezione mucosa, prurito e lacrimazione.
La patologia allergica è caratterizzata da iperproduzione di IgE, in particolare IgE specifiche verso antigeni (allergeni) che sensibilizzano specificamente il sistema immune del soggetto predisposto alle reazioni atopiche. I soggetti con patologia allergica hanno di solito un aumentato numero di IgE e, soprattutto, hanno IgE specificamente dirette contro un particolare allergene. Il processo di sensibilizzazione inizia in una epoca molto precoce della vita ma può avvenire in ogni momento a seconda dei vari allergeni incontrati.
La risposta IgE mediata meglio caratterizzata è l’interazione tra IgE e recettore ad alta affinità (FceRI) presente sulla superficie dei mastociti (cellule infiammatorie primarie) . Quando molecole di IgE legate alle cellule legano in modo crociato un allergene attivano il mastocita. Questa attivazione avviene con una degranulazione ed il rilascio di vari mediatori e citochine proinfiammatorie preformate o neogenerate come istamina, interleuchine, leucotrieni e prostaglandine. Questa è la classica reazione di ipersensibilità di I tipo della cascata infiammatoria-allergica. Le citochine derivate dai mastociti possono contribuire alla risposta infiammatoria cronica attraendo gli eosinofili al tessuto bersaglio.
Questi ultimi, a loro volta, rilasciano altri mediatori rpoinfiammatori . Alcuni di questi mediatori causano infiammazione ed alcuni hanno anche proprietà citolesive. La presenza del recettore FceRI su vari altri tipi cellulari può contribuire inoltre a varie attività infiammatorie. Questi recettori ad alta affinità si ritrovano soprattutto su mastociti e basofili nonché sulle cellule dendritiche, che agiscono come cellule che presentano l’antigene.
Livelli di IgE sieriche sono collegati a wheezing persistente (equivalente di asma)
I sibili respiratori, avvertibili con il fonendoscopio ma spesso anche udibili nell’ambiente, sono comuni nell’infanzia e la causa più comune sono le infezioni virali. Nei bambini asmatici i sibili persistenti, soprattutto di notte e durante sforzi fisici (soprattutto corsa) si pensa siano dovuti ad una latente risposta infiammatoria IgE-mediata verso gli allergeni sensibilizzanti . L’alta correlazione tra i sibili persistenti ed i livelli elevati di IgE suggerisce il substrato allergico-atipico dell’asma, che viene poi confermato con i test allergologici in vivo (prick test) o in vitro (RAST e suoi equivalenti).
In uno studio su bambini con sibili persistenti e precoce sensibilizzazione ad aeroallergeni, la maggior parte di questi aveva alti livelli di IgE ad un’età precoce (inrtrno all’anno).
Ciò suggerisce che la predisposizione a rispondere a stimoli ambientali con alti livelli di IgE precede la sensibilizzazione precoce. Negli atopici si determina quindi verosimilmente un difetto comune nello sviluppo del sistema immune che coinvolge sia la produzione di IgE sia la sensibilizzazione allergica precoce . Non sempre però i test cutanei o in vitro sono positivi prima dei 4-5 anni, per i tempi della risposta immunologica e la sua evidenziazione.

L’importanza dei livelli di IgE
Essendo molto variabile nella popolazione normale il livello delle IgE sieriche non vi è accordo nel definire i livelli di normalità. Le IgE sieriche hanno un picco durante l’infanzia, decrescono con l’età e possono essere diversi nei due sessi (significativamente più basse nella donna che nell’uomo).
Le IgE costituiscono il mediatore chiave dell’infiammazione allergica delle mucose delle vie aeree. La riduzione dei livelli di IgE costituisce un obiettivo importante per prevenire l’infiammazione e tutti i suoi effetti avversi.
Un modo per raggiungere questo obiettivo potrebbe essere la produzione di uno specifico anticorpo anti-IgE. Questo è stato sviluppato con successo oggi e il risultato è Xolairâ (omalizumab-rhuMAb/E25).
Xolair (omalizumab)
Xolair (omalizumab) è il capostipite di una nuova classe di farmaci che ha come bersaglio specifico le IgE.
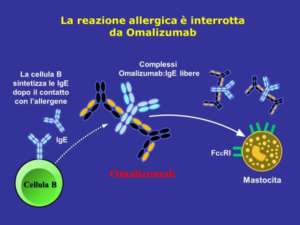
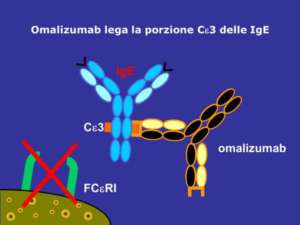
Xolair è un anticorpo monoclonale ricombinante umanizzato anti-IgE che si lega alle IgE libere e di conseguenza previene la risposta IgE-mediata . Dal legame e dalla formazione del complesso con una IgE libera, Xolair ferma la cascata allergica che causa i sintomi allergici.
La molecola (omalizumab) è stata sviluppata usando una struttura di IgG sulla quale è stata impiantata la regione determinante della complementarietà ottenuta da un anticorpo anti-IgE di topo. L’anticorpo monoclonale umanizzato , che viene somministrato per via sottocutanea, con una modalità ben accettata dai pazienti, a dosi dipendenti dalla concentrazione ematica di IgE e dal peso corporeo del soggetto, contiene solo il 5% di residui aminoacidici non umani, rendendo in tal modo minimo il rischio potenziale di una risposta immune nei confronti di proteine non-self. Ciò migliora il profilo di sicurezza, l’efficacia terapeutica e la farmacocinetica, dandogli una emivita di circa 3 settimane in vivo. Ciò permette un dosaggio mensile o trisettimanale.
Xolair si somministra attraverso iniezioni sottocutanee e la “compliance” del paziente verso il trattamento è davvero buona.
Di fatto la terapia con anti-IgE ha consentito di far migliorare, spesso in modo eclatante, la sintomatologia asmatica IgE-dipendente in soggetti con asma atopico di tipo grave da allergeni perenni, migliorando frequentemente in modo evidente la loro qualità di vita.
Treating severe allergic asthma with anti-IgE monoclonal antibody (omalizumab): a review.
D’Amato G, Stanziola A, Sanduzzi A, Liccardi G, Salzillo A, Vitale C, Molino A, Vatrella A, D’Amato M.
Multidiscip Respir Med. 2014 Apr 15;9(1):23. doi: 10.1186/2049-6958-9-23. eCollection 2014. Review.
D’Amato G, Perticone M, Bucchioni E, Salzillo A, D’Amato M, Liccardi G.
Eur Ann Allergy Clin Immunol. 2010 Aug;42(4):135-40. Review.
Select item 186005943.
World Asthma and COPD Forum. Clinical trial results with omalizumab.
D’Amato G.
IDrugs. 2008 Jul;11(7):489-92. No abstract available.
D’Amato G, Salzillo A, Piccolo A, D’Amato M, Liccardi G.
Ther Clin Risk Manag. 2007 Aug;3(4):613-9.
D’Amato G, Piccolo A, Salzillo A, Noschese P, D’Amato M, Liccardi G.
Recent Pat Inflamm Allergy Drug Discov. 2007 Nov;1(3):225-31. Review.
.
D’Amato G, Bucchioni E, Oldani V, Canonica W.
Treat Respir Med. 2006;5(6):393-8.
.
D’Amato G.
Eur J Pharmacol. 2006 Mar 8;533(1-3):302-7. Epub 2006 Feb 7. Review.
.
D’Amato G, Liccardi G, Noschese P, Salzillo A, D’Amato M,
Curr Drug Targets Inflamm Allergy. 2004 Sep;3(3):227-9. Review.
.
Anti-IgE monoclonal antibody: a new approach to the treatment of allergic respiratory diseases.
D’Amato G, Oldani V, Donner CF.
Monaldi Arch Chest Dis. 2003 Jan-Mar;59(1):25-9. Review.
.
Therapy of allergic bronchial asthma with omalizumab – an anti-IgE monoclonal antibody.
D’Amato G.
Expert Opin Biol Ther. 2003 Apr;3(2):371-6. Review.
Treating atopic asthma with the anti-IgE monoclonal antibody.
D’Amato G.
Monaldi Arch Chest Dis. 2002 Apr;57(2):117-9. Review.




